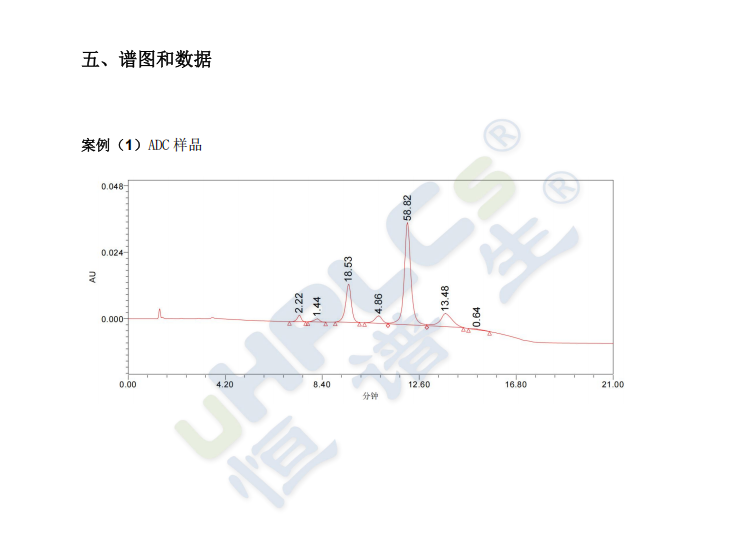
ADC药物分离难题的终极答案:恒谱生BioM系列 HIC-Butyl疏水色谱柱!
在抗体偶联药物(ADC)的研发与质控征程中,分析科学家们常常面临一座难以逾越的大山:如何对结构极其复杂的ADC分子进行高效、精准的分离与表征?ADC由抗体、连接子和细胞毒性药物三部分构成,这种异质性导致了其在疏水性、电荷和分子大小上存在巨大差异,从而产生了一系列的“分离难题”:
难题一:分辨率不足。 传统的SEC或IEX方法难以有效区分载药量不同(DAR值)的ADC物种,以及裸抗、未偶联的小分子药物等,色谱峰重叠严重,信息模糊。
难题二:活性丧失风险。 某些分离条件可能过于剧烈,导致ADC分子变性、聚集或降解,无法反映其真实的体内状态。
难题三:方法重现性差。 色谱柱批次间的差异可能导致分析方法转移失败,严重影响从研发到生产放大的进程。
面对这些挑战,恒谱生BioM系列 HIC-Butyl疏水色谱柱,凭借其独特的作用机理和精准的设计,正成为破解ADC药物分离难题的“终极答案”。
一、HIC原理:为何它是ADC分析的“天生一对”?
疏水相互作用色谱(HIC)的原理,完美契合了ADC药物的特性。在高盐浓度下,ADC分子表面的疏水区域会与色谱柱固定相发生可逆的相互作用。疏水性越强的物种(通常是小分子药物载量越高的ADC),与固定相的结合就越紧密,从而在洗脱时保留时间越长。
这种基于天然疏水性的分离机制,具有两大无可比拟的优势:
保持生物活性: 整个过程在温和的水相缓冲体系中进行,无需使用可能导致蛋白变性的有机溶剂,最大程度地保持了ADC药物的完整构象和生物活性。
卓越的选择性: 能够精准地依据DAR值的微小差异进行分离,将DAR0. DAR2. DAR4. DAR6等不同载药量的组分清晰分开,为DAR值测定和纯度鉴定提供了坚实基础。
二、恒谱生HIC-Buty的“终极答案”体现在何处?
仅仅理解HIC原理还不够,关键在于如何将原理转化为稳定、可靠、高性能的产品。恒谱生HIC-Buty疏水色谱柱通过以下核心设计,将“解决方案”落实到了每一个细节:
1. 精准的丁基键合与低吸附表面
我们的色谱柱采用高纯度硅胶基质,通过精确控制的丁基键合技术,在表面形成均一、适度的疏水层。这种“丁基”链长的选择,在疏水捕获能力和温和洗脱之间取得了最佳平衡。更重要的是,我们创新的表面键合技术 极大地降低了硅胶基质表面与生物大分子之间的非特异性吸附。这意味着ADC样品在柱上的损失更少,从而实现了高样品回收率——确保您检测到的每一个峰,都能真实反映样品中各组分的含量。
2. 为生物大分子量身定制的传质空间
ADC分子尺寸庞大,传统的小孔径色谱柱会造成传质阻力大、柱压高、峰形展宽等问题。恒谱生HIC-Butyl疏水色谱柱采用了1000Å(埃)的大孔径设计,为ADC等生物大分子提供了充足的进入和扩散空间。结合5μm的单分散微球,确保了溶质在流动相和固定相之间能够快速传质,最终实现了高柱效和尖锐的峰形,使得紧密相邻的ADC组分也能被清晰分辨。
3. 将“一致性”刻入产品基因
我们深知,对于方法转移和长期质控而言,色谱柱的批间一致性至关重要。恒谱生从原料筛选到最终封装,执行严格的质量控制体系。每一批次的HIC-Buty柱在保留时间、柱效和选择性等关键参数上都保持高度一致。当您的分析方法需要从研发实验室转移到生产QC部门,或在不同地区的实验室间进行复现时,HIC-Buty能为您扫除因色谱柱差异带来的障碍,确保结果的可靠与可比。
三、应用实例:从混沌到清晰
在实际应用中,使用HIC-Butyl色谱柱分析一款ADC药物,通常能获得一张令人振奋的色谱图:在优化的盐梯度下,裸抗体(DAR0)首先被洗脱,随后DAR2、DAR4等组分依次出峰,峰形对称且基线分离。这张清晰的图谱,不仅可以直接用于计算平均DAR值,还能精确量化各组分所占的比例,为工艺优化和质控标准制定提供了无可争议的数据支持。
ADC药物的分离难题,根源在于其固有的复杂性。恒谱生HIC-Butyl疏水色谱柱,凭借其对HIC原理的深刻理解、为生物大分子量身定制的物理参数(1000Å孔径,5μm粒径),以及确保结果可靠的关键技术(高选择性、高回收率、出色一致性),提供了一个从原理到实践都经得起考验的完整解决方案。它不仅是您实验室中的一件工具,更是您攻克ADC分析壁垒,加速药物开发进程的终极答案。
发布于: 2025-11-19