HPLC分析-缓冲盐如何选择?
在高效液相色谱分析中,缓冲盐的选择往往是“看不见的胜负手”。选对了,分离度好、峰形对称、重现性佳;选错了,拖尾、基线漂移、保留时间飘忽不定,甚至色谱柱报废都找上门来。
那么,面对磷酸盐、甲酸铵、乙酸铵、三氟乙酸等五花八门的缓冲体系,到底该怎么选?今天,我们用一篇干货,帮你彻底理清 HPLC 缓冲盐选择的底层逻辑与实操流程。
一、缓冲盐三大“使命”
01 稳定pH,锁定分析物形态
可解离的酸性或碱性化合物,在不同的pH下会以分子态或离子态存在,直接决定其在色谱柱上的保留行为,电离形式的化合物极性高,在反相柱上保留弱;而非电离形式则疏水性强,保留时间长。缓冲盐通过共轭酸碱对的调节,抑制电离,将pH波动控制在±0.05以内,确保保留时间稳定重现。
02 抑制硅羟基效应,改善峰形
硅胶色谱柱表面残留的硅羟基,在偏碱性条件下会解离带负电,与带正电的碱性化合物发生离子交换,导致严重峰拖尾。缓冲盐中的阳离子能有效屏蔽硅羟基,从根源上减少拖尾、分叉。
03 调控离子强度,优化分离度
缓冲盐浓度影响分析物与固定相之间的疏水相互作用,微调不同化合物的保留行为,提升分离度。
二、”五步”挑选缓冲盐
01 确认检测器
LC-MS/ELSD:必须使用挥发性缓冲盐,如甲酸铵、乙酸铵、甲酸、乙酸等。磷酸盐、硼酸盐等非挥发性盐禁止使用,否则会严重污染离子源、抑制信号,甚至损坏质谱仪。
UV/PDA:非挥发性盐和挥发性盐均可使用。但需注意缓冲盐的紫外截止波长应低于检测波长20 nm以上,否则会产生基线噪音和漂移。
02 确定目标pH
黄金法则:让分析物以单一形态存在,即流动相pH应偏离分析物pKa±2个单位以上。此时,微小pH波动不会造成保留时间剧烈变化。
● 酸性化合物(pKa 3-6)
pH<pka-2时呈分子态,保留增强;ph>pKa+2时解离为离子,保留减弱。
● 碱性化合物(pKa 8-11)
pH>pKa+2时呈分子态,保留增强;pH<pka-2时呈离子态,保留减弱且易拖尾。< p=”">
● 中性化合物
pH几乎不影响保留。
03 确定缓冲盐体系
目标pH必须落在缓冲盐的有效缓冲范围(pKa±1)内,越接近pKa,缓冲能力越强。
04 确定浓度
● 常规UV检测:10-50 mmol/L,最常用20 mmol/L,兼顾缓冲能力与盐析风险。
● 改善峰拖尾:可提升至30-50 mmol/L,增强对硅羟基的屏蔽效果。
● 梯度洗脱:优先选择10-20 mmol/L,降低高有机相比例下的盐析风险。
● LC-MS检测:5-20 mmol/L,推荐10 mmol/L,高浓度会导致离子抑制和离子源污染。
05 方法验证
● 盐析测试:缓冲液与最高比例有机相等体积混合,静置10 min无沉淀。
● 紫外兼容性:目标波长下吸光度<0.05 AU。
● 梯度基线:漂移可接受,确保水相和有机相缓冲盐浓度对等。
● 重现性:连续5针进样,目标峰保留时间RSD ≤ 2.0%。
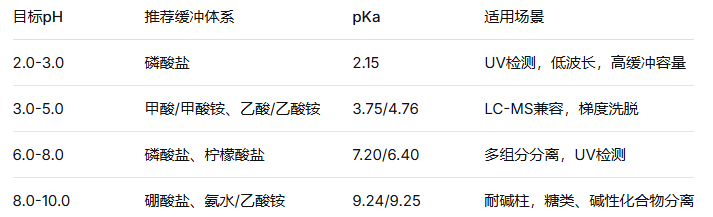
三、常见缓冲盐体系
1、非挥发性盐(仅用于 UV)
● 磷酸盐:紫外截止波长 < 200 nm,缓冲范围广,成本低,但不可用于 MS,高有机相易盐析。
● 柠檬酸盐:多 pKa 覆盖连续范围,可改善峰形,但紫外截止波长~230 nm,易滋生微生物。
● 硼酸盐:适配高 pH,对糖类有特殊选择性,但不可用于 MS,与多元醇络合。
2、挥发性盐(LC-MS 首选)
● 甲酸铵 / 乙酸铵:MS 全模式兼容,双缓冲范围,溶解度优异,是 LC-MS 常规分析的主力军。
● 甲酸 / 乙酸:挥发性极佳,无盐析风险,但单独使用缓冲容量有限,常与铵盐联用。
● 三氟乙酸(TFA):强酸性,兼具离子对作用,可显著改善多肽蛋白峰形,但强离子抑制,LC-MS 慎用。
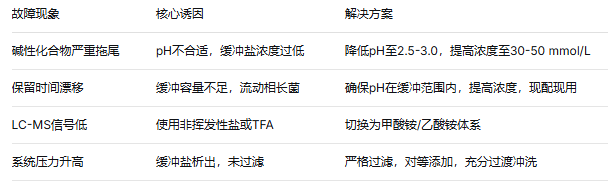
四、常见错误
缓冲盐的选择看似复杂,实则“有法可依”。掌握“先定检测器、再定pH、匹配体系、优化浓度、验证风险”的五步法,你也能在HPLC方法开发中游刃有余,跑出稳定又漂亮的色谱图。
如果你在实验中还遇到过什么“奇葩”的缓冲盐问题,欢迎留言讨论!
发布于: 2026-03-31